В Израиле объяснили: вакцина против "Омикрона" будет нужна и после пятой волны
В ближайшие недели компания Pfizer должна обратиться в Федеральное управление США по надзору за качеством пищевых продуктов и медикаментов (FDA) за экстренным разрешением на использование вакцины против коронавируса, модицфиированной для борьбы со штаммом «Омикрон». Возможно, аналогичное обращение поступит и от компании Moderna.
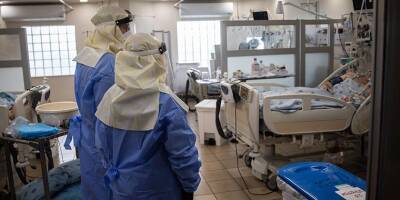
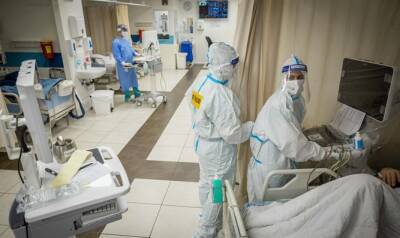
Тем временем пятая волна пандемии, вызванная распространением «Омикрона», постепенно сходит на нет, правительства многих стран отменяют карантинные ограничения. Существует ли реальная необходимость в модифицированной вакцине? В понедельник, 14 февраля, Ynet обратился к специалисту за ответом на этот вопрос.
Но прежде напомним о том, что вакцина Pfizer создана с помощью революционной технологии mRNA, позволяющей не только повысить степень защиты организма от инфекции, но и перестроить саму вакцину, адаптируя ее к новым вариантам вируса. В конце 202 года нам обещали, что на модификацию вакцины уйдет всего 6 недель. Однако «Омикрон» появился почти 3 месяца тому назад, а новой вакцины до сих пор нет.
Дело не в производстве вакцины, а в продолжительности клинических испытаний. Новый вариант вакцины сперва испытали на животных, теперь испытывают на людях. Прежде чем обращаться в FDA, необходимо убедиться в безопасности и эффективности прививки новой вакциной. Как сообщали «Вести», испытания будут проводиться и в Израиле.
FDA выдает экстренное разрешение не сразу, а лишь после ознакомления с материалами исследований. Если Pfizer обратится за лицензией в конце февраля или начале марта, разрешение будет получено в апреле, а то и в мае. Будет ли нужна модифицированная вакцина через 2-3 месяца, когда, согласно большинству прогнозов, пятая волна завершится?
Проф. Лиор Нешер, специалист по инфекционным
 vesty.co.il
vesty.co.il